Antígenos
Como se mencionó anteriormente, originalmente se consideraba un antígeno a una molécula que se liga específicamente a un anticuerpo; ahora, un antígeno se define como cualquier molécula o fragmento molecular que puede ser reconocido por una gran variedad de receptores antigénos (receptores de células T o receptores de células B ) del sistema inmune adaptado.
Las células presentan antígenos al sistema inmune mediante a través de moléculas de histocompatibilidad (CMH). Dependiendo del antígeno presentado y del tipo de molécula de histocompatibilidad, se pueden activar diferentes tipos de leucocitos. Por ejemplo, para el reconocimiento por parte de los receptores de células T (TCR), los antígenos (mayoritariamente proteínas) deben ser procesado a pequeños fragmentos dentro de la célula y presentados al receptor de células T por el complejo mayor de histocompatibilidad.
Los antígenos por sí solos no son capaces de provocar una respuesta inmune protectora sin la ayuda de un adyuvante inmunológico. Los componentes adyuvantes de las vacunas juegan un papel esencial para la activación del sistema inmune innato. Un inmunógeno es entonces, en analogía al antígeno, una sustancia (o una combinación de sustancias) capaz de desencadenar una respuesta inmune protectora cuando éste es introducido al organismo.
Un inmunógeno debe iniciar una respuesta inmune innata, para más adelante continuar con la activación del sistema inmune adaptativo, mientras que un antígeno es capaz de unirse a los productos immunoreceptores altamente variables (receptores de células T o receptores de células B ) una vez que estos han sido producidos. Los conceptos superpuestos de inmunogenicidad y antigenicidad son, por lo tanto, ligeramente diferentes,
Los antígenos son usualmente proteínas o polisacáridos. Esto incluye partes de bacterias (cápsula, pared celular, flagelos, fimbrias, y toxinas), de virus y otros microorganismos. Los lípidos y ácidos nucleicos son antigénicos únicamente cuando se combinan con proteínas y/o polisacáridos. Los antígenos no-microbianos exógenos (ajenos al individuo) pueden incluir polen, clara de huevo, y proteínas de tejidos y órganos trasplantados, o proteínas en la superficie de glóbulos rojos transfundidos. Las vacunas son un ejemplo de antígenos en una forma inmunogénica; estos antígenos son intencionalmente administrados para inducir el fenómeno de memoria del sistema inmune adaptativo hacia los antígenos que invaden al receptor.
Aunque la estructura general de todos los anticuerpos es muy semejante, una pequeña región del ápice de la proteína es extremadamente variable, lo cual permite la existencia de millones de anticuerpos, cada uno con un extremo ligeramente distinto. A esta parte de la proteína se la conoce como región hipervariable. Cada una de estas variantes se puede unir a una "diana" distinta, que es lo que se conoce como antígeno.
Esta enorme diversidad de anticuerpos permite al sistema inmune reconocer una diversidad igualmente elevada de antígenos. La única parte del antígeno reconocida por el anticuerpo se denomina epítopo. Estos epítopos se unen con su anticuerpo en una interacción altamente específica que se denomina adaptación inducida, que permite a los anticuerpos identificar y unirse solamente a su antígeno único en medio de los millones de moléculas diferentes que componen un organismo.
El reconocimiento de un antígeno por un anticuerpo lo marca para ser atacado por otras partes del sistema inmunitario. Los anticuerpos también pueden neutralizar sus objetivos directamente, mediante, por ejemplo, la unión a una porción de unpatógeno necesaria para que éste provoque una infección.
La extensa población de anticuerpos y su diversidad se genera por combinaciones al azar de un juego de segmentosgenéticos que codifican diferentes lugares de unión al antígeno (o paratopos), que posteriormente sufren mutacionesaleatorias en esta zona del gen del anticuerpo, lo cual origina una diversidad aún mayor.
Los genes de los anticuerpos también se reorganizan en un proceso conocido como conmutación de clase de inmunoglobulina que cambia la base de la cadena pesada por otra, creando un isotipo de anticuerpo diferente que mantiene la región variable específica para el antígeno diana. Esto posibilita que un solo anticuerpo pueda ser usado por las diferentes partes del sistema inmune. La producción de anticuerpos es la función principal del sistema inmunitario humoral.
 |
Origen de los Antígenos
-Antígenos exógenos=
Los antígenos exógenos son antígenos que han entrado al cuerpo desde el exterior, por ejemplo mediante inhalación, ingestión o inyección. A menudo, la respuesta inmune hacia antígenos exógenos es subclínica. Estos antígenos son tomados en las células presentadoras de antígenos (CPAs) mediante endocitosis o fagocitosis, y procesadas en fragmentos. Las CPAs entonces presentarán esos fragmentos a linfocitos T colaboradores (CD4+) con ayuda de moléculas de histocompatibilidad de clase II en su superficie. Los linfocitos T que reconocen de manera específica la dupla péptido:CMH son activados y comenzarán a secretar citocinas. Las citocinas son sustancias que a su vez pueden activarlinfocitos T citotóxicos (CD8+), células productoras de anticuerpos o linfocitos B, macrófagos, y otras.
Algunos antígenos entran al organismo como antígenos exógenos, para después pasar a ser antígenos endógenos (por ejemplo, un virus intracelular). Los antígenos intracelulares pueden ser liberados de nuevo al torrente sanguíneo una vez que la célula infectada sea destruida.
-Antígenos endógenos=
Los antígenos endógenos son aquellos antígenos que han sido generados al interior de una célula, como resultado delmetabolismo celular normal, o debido a infecciones virales o bacterianas intracelulares. Los fragmentos de esos antígenos son presentados sobre la superficie celular en un complejo con moléculas MHC de clase I. Si son reconocidos por linfocitos T cito tóxicos (CD8+) activados, éstos comenzarán a secretar varias toxinas que causarán la lisis o apoteosis (muerte celular) de la célula infectada. Para prevenir que las células cito tóxicas destruyan células normales que presenten proteínas propias del organismo, éstos linfocitos T autoreactivos son eliminados del repertorio como resultado de la tolerancia (también conocida como selección negativa). Los antígenos endógenos comprenden a los antígenos xenógenicos (heterólogos), autólogos, idiotípicos y alogénicos (homólogos).
-Autoantigeno=
Un autoantígeno se refiere a una proteína normal o un complejo de proteínas, algunas veces también ADN o ARN, que son reconocidos por el sistema inmune. Ocurre en pacientes que sufren de alguna enfermedad autoinmune específica. Estos antígenos no deberían, en condiciones normales, activar el sistema inmune, pero en estos pacientes, debido principalmente a factores genéticos y/o ambientales, se ha perdido una correcta tolerancia inmunológica.
Estructura Básica de los Anticuerpos
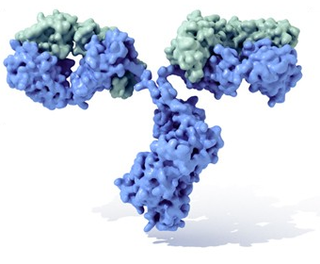
con independencia de la clase a la que pertenece, cualquier anticuerpo tiene una estructura básica que consiste en cuatro cadenas polipéptidas serpenteantes unidas unas a otras por enlaces azufre-azufre (disulfuro), vea la figura 1 a la derecha. Dos de esas cadenas, conocidas como cadenas pesadas, son idénticas mutuamente y presentan unos 400 amino ácidos (representadas con tonos de rojo en la figura 1). Las otras dos, o cadenas ligeras (representadas con tonos de azul), son igualmente idénticas entre ellas pero tienen una longitud alrededor de la mitad que las pesadas. Las cadenas pesadas, en su zona más o menos central, tienen una "bisagra" flexible. Observe en la figura 1 que los enlaces azufe-azufre no solo unen las cadenas entre sí, si no que también enlazan juntos ciertos amino ácidos dentro de las cadenas pesadas y ligeras. Los enlaces azufre-azufre dentro de una misma cadena se producen cada unos 110 amino ácidos de distancia, lo que hace que la parte entre ellos de la cadena se doble formando un bucle.
Cuando las cuatro cadenas se combinan de la forma descrita forman una molécula conocida comomonómero (de anticuerpo) con dos mitades idénticas y cada una consistente en dos cadenas pesadas y dos ligeras. La molécula en conjunto puede tener forma de T o de Y.
Cada una de las cuatro cadenas que forman el anticuerpo presentan dos zonas diferenciables en un extremo, que es diferente de unos anticuerpos a otros, y conocida como región variable (V); y otra mucho mayor región constante (C) en el otro extremo que es igual (o casi igual) para todos los anticuerpos de una misma clase. Las regiones variables de las cadenas pesada y ligera se combinan para dar lugar a la zona de enlace del antígeno, especializadas para unirse a un determinado tipo de antígeno o a un determinante antigénico. Ello implica que cada monómero de anticuerpo tiene dos de tales regiones de enlace.
 |
formación de los macrofagos
Los macrófagos proceden de los monocitos. Estos se forman en la médula óseaprocedentes de células pluripotenciales de la serie granulocítico-monocítica, gracias al factor de crecimiento GM-CSF(granulocyte macrophage colony stimulating factor) y otras citoquinas como la interleucina 3 (IL-3).
Cuando estos factores de crecimiento están presentes en la médula ósea, la célula progenitora prolifera y se diferencia apromonocitos, células que en divisiones celulares posteriores producirán monocitos.
La diferenciación celular de la célula madre está asociada con la expresión de receptores de membrana para citocinasespecíficas. Los monocitos permanecen en la médula ósea menos de 24 horas, después pasan a la circulación sanguíneay son distribuidos por todo el cuerpo. En esta etapa, se visualizan al microscopio en los frotis de sangre periférica como células de mayor tamaño, cuyo diámetro oscila entre 15 a 30 y poseen una alta relación núcleo/citoplasma.
En adultos sanos normales, la vida media de un monocito circulante se estima en 70 horas y en una proporción del 1 al 6 % del total de leucocitos en un recuento normal en sangre periférica.
Una vez los monocitos salen de los capilares sanguíneos y se localizan en los tejidos se transforman en macrófagos. Esta diferenciación de monocito a macrófago afecta a gran cantidad de cambios como que la célula aumenta su tamaño de 5 a 10 veces, sus orgánulos incrementan tanto su número como su complejidad, adquiere capacidad fagocítica, produce altas concentraciones de enzimas líticas y empieza a secretar gran variedad de substancias solubles que realizan diferentes funciones.
Los macrófagos están habitualmente en estado de reposo, pueden ser activados por gran variedad de estímulos durante la respuesta inmune. La fagocitosis de antígenos sirve como estímulo inicial; sin embargo, los macrófagos y su actividad pueden aumentarse por citocinas secretadas por linfocitos T colaboradores, o mediante el contacto con los mismos. Uno de los más potentes activadores de macrófagos es el interferón gamma. También son capaces de reconocer Patrones moleculares asociado a patógenos.
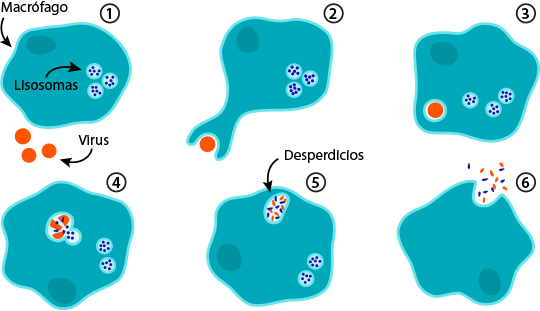
Fagocitosis:
la función principal de los macrófagos es la de fagocitar todos los cuerpos extraños que se introducen en el organismo como las bacterias y sustancias de desecho de los tejidos. Los macrófagos son fagocitos junto con losneutrófilos y otras células. Los macrófagos tienen la capacidad de quimiotaxis, es decir la de ser atraídos y desplazados hacia una determinada localización por la presencia de determinados factores quimiotácticos para monocitos comointerleucina-I, trombina, factor de crecimiento derivado de las plaquetas, factor del complemento C5a, fragmentos decolágeno, elastina, fibronectina, calicreína, activador del plasminógeno, inmunoglobulinas y leucotrienos.
 |
Inflamación:
Los macrófagos forman parte del Sistema inmunitario innato, es decir, inician una respuesta natural contra los microorganismos, porque los macrófagos expresan receptores de membrana para numerosas moléculas bacterianos, por ejemplo: receptor para lipopolisacáridos (CD14), receptores C11b/CD18, receptores para manosas, y receptor para glúcidos entre otros. Los macrófagos de los vertebrados y de los invertebrados participan en gran medida de la respuesta inmune innata a infecciones gracias a sus receptores "scavengers", o barredores, que poseen una especificidad a ligandos muy amplia como: lipoproteínas, proteínas, poli y oligonucleótidos, polisacáridos aniónicos,fosfolípidos y otras moléculas.
Presentación de antígenos: cuando los macrófagos fagocitan un microbio, procesan y sitúan sus antígenos en la superficie externa de su membrana plasmática, donde serán reconocidos por los linfocitos T colaboradores; tras el reconocimiento, los T producen linfoquinas que activan a los linfocitos B. Por eso los macrófagos forman parte de las llamadas células presentadoras de antígenos, ya que poseen en sus membranas moléculas del complejo mayor de histocompatibilidad (MHC) de clase II. Los linfocitos B activados producen y liberan anticuerpos específicos a los antígenos presentados por el macrófago. Estos anticuerpos se adhieren a los antígenos de los microbios o de células invadidas por virus y así atraen con mayor avidez a los macrófagos para fagocitarlos.
Reparación de tejidos: Los macrófagos además ingieren células muertas del anfitrión y participan en la reparación de tejidos dañados trás la reacción inmunitaria.
Hemostasia:
el macrófago produce una serie de sustancias que participan en la coagulación como son: proteína C,trombomodulina, factor tisular, factor VII, factor XIII y el inhibidor del activador del plasminógeno.
Fagocitos
Los fagocitos son células presentes en la sangre y otros tejidos animales capaces de captar microorganismos y restos celulares (en general, toda clase de partículas inútiles o nocivas para el organismo) e introducirlos en su interior con el fin de eliminarlos, en un proceso conocido como fagocitosis. Su nombre procede delgriego phagein y -cito, sufijo utilizado con el significado de 'célula', procedente del término kutos (κύτος, 'cavidad, urna').Existen muchos tipos decélulas capaces de efectuar la fagocitosis; las células del sistema inmune que la realizan son de vital importancia en la defensa del organismo contra lasinfecciones.
 |
Están presentes en todos los animales y se encuentran muy desarrollados en los vertebrados. Un litro de sangre humana contiene alrededor de seis mil millones de estas células. Fueron descubiertos en 1882 en larvas de estrellas de mar por Ilya Ilyich Mechnikov. Debido a este trabajo, Mechnikov fue galardonado con el Premio Nobel en Fisiología o Medicina en 1908. También se encuentran presentes en especies no animales; de hecho, algunas amebas poseen un comportamiento similar a los macrófagos (un tipo de fagocitos), lo que sugiere que aparecieron en una fase temprana de la evolución.
En sentido genérico, suele llamarse «fagocitos» a las células del sistema inmunecon capacidad fagocítica (como los macrófagos). Siendo más precisos, no todos los fagocitos son glóbulos blancos o células inmunitarias: en humanos y otros animales se clasifican en «profesionales» y «no profesionales», dependiendo de su efectividad y de si poseen funciones distintas a la fagocitosis.Los fagocitos profesionales incluyen a los neutrófilos, monocitos, macrófagos, células dendríticas y mastocitos[cita requerida]; los fagocitos no profesionales incluyen elementos muy numerosos en el cuerpo humano y distintos a los leucocitos, como las células epiteliales, endoteliales, fibroblastos y células del mesénquima. La diferencia fundamental entre los dos tipos es que los profesionales poseen receptores celulares en su superficie que son capaces de distinguir entre sustancias propias y ajenas al cuerpo. Esta especificidad es la base del reconocimiento de lo propio frente a lo ajeno, y sustenta la defensa contra las infecciones mediada por el sistema inmune y el remodelado de los tejidos sanos (retirando las células muertas o no funcionales).
La fagocitosis es el proceso de captura de partículas en el interior de una célula, ya sean bacterias, parásitos, células apoptóticas; en definitiva, toda clase de partícula extraña. Involucra a varios procesos moleculares.Se produce cuando estos elementos se unen a receptores de la superficie del fagocito, cambiando su estructura tridimensional e induciendo la inclusión de la partícula en el interior de la célula. En el caso de los neutrófilos humanos, la fagocitosis de bacterias se produce por término medio en nueve minutos. Cada célula fagocítica posee un compartimento celular denominado fagosoma (en el que se almacena la partícula a eliminar) cuyo destino celular es la fusión con un lisosoma o gránulo para formar unfagolisosoma; en el caso de los neutrófilos humanos, la fusión sucede en un minuto.
 |
El orgánulo generado posee una batería de métodos enzimáticos que produce casi en todos los casos la muerte del elemento fagocitado en cuestión de minutos.Las células dendríticas y los macrófagos no son tan efectivos como los neutrófilos y pueden prolongar el proceso hasta varias horas. Los macrófagos son lentos y, frecuentemente, expulsan el material a medio digerir al medio circundante; esta emisión atrae (recluta) a más fagocitos. Los elementos fagocitados son muy diversos: algunas técnicas científicas consisten en la inducción de fagocitosis de incluso limaduras de hierro (de esta manera y empleando un imán es posible separar los fagocitos activos del resto de células y otros materiales).
 |
Cada fagocito posee varios tipos de receptores en su superficie que reconocen las partículas a fagocitar y que desencadenan el proceso de fagocitosis. Entre ellos se encuentran las opsoninas, receptores tipo Scavenger y receptores de tipo Toll(TLRs). Las opsoninas activan la fagocitosis de bacterias recubiertas de Ig G o mediante proteínas del complemento (las cuales se activan mediante una cascada enzimática que favorecen la destrucción de elementos extraños en la sangre). Los receptores tipo Scavenger reconocen una gran diversidad de moléculas de la superficie bacteriana. Los receptores de tipo Toll inducen la respuesta inflamatoria además de la fagocitosis; su nombre deriva de los receptores tipo Toll deDrosophila melanogaster, con quienes guardan cierta homología.
 |
Caracteristicas de las celulas b1
Las células B1, responsables de la producción de IgM sérica, constituyen una población de linfocitos B con ubicación anatómica y características fenotípicas y funcionales particulares10. Los linfocitos B1 se ubican mayoritariamente en cavidad peritoneal y pleural 11 y presentan el fenotipo B220lowIgMhiCD23low/-CD43+IgDlow. Estas células presentan características de células activadas y son de mayor tamaño y complejidad citoplasmática que las células B2 12,13 .
Las células B1, responsables de la producción de IgM sérica, constituyen una población de linfocitos B con ubicación anatómica y características fenotípicas y funcionales particulares10. Los linfocitos B1 se ubican mayoritariamente en cavidad peritoneal y pleural 11 y presentan el fenotipo B220lowIgMhiCD23low/-CD43+IgDlow. Estas células presentan características de células activadas y son de mayor tamaño y complejidad citoplasmática que las células B2 12,13 .
Dentro de las células B1 se distinguen dos subpoblaciones: la de los linfocitos B1a que expresan el marcador pan-T, CD5, y aquella que no lo expresa correspondiente a los linfocitos B1b. Sin embargo, los linfocitos B1a y B1b son similares en cuanto a la expresión de los otros marcadores de la superficie celular, 15. Los linfocitos B1a son numéricamente superiores a los B1b y es por ello que la mayoría de la información disponible sobre los linfocitos B1 se refiere a la población B1a. En esta revisión, se aclarará específicamente, cuando se disponga de la información, de que tipo de linfocitos B1 se trata.
En el ratón adulto, los linfocitos B1 están restrictos a cavidad peritoneal aunque existe una pequeña proporción de estas células en bazo11. Los linfocitos B1 de cavidad peritoneal expresan, en forma constitutiva, el factor de transcripción STAT-3 fosforilado mientras que las células B2 y B1 de bazo sólo lo expresan cuando se activan. Por lo tanto, la expresión de STAT-3 fosforilado en la población de células B1 depende de la localización anatómica de las mismas16. Las células B1 de bazo, en ratones, comparten ciertas características fenotípicas con las células B1 de peritoneo, pero son más parecidas a las células B2 esplénicas en cuanto a la expresión de STAT-3, CREB, y PU.1, y también en las señales requeridas para progresar en el ciclo celular16. Uno de los aspectos más relevantes de las células B1 peritoneales murinas es quizás su capacidad de autorrenovación, ya que producen y liberan IL-10, factor autócrino que media la proliferación y sobrevida de las mismas
No hay comentarios:
Publicar un comentario